Змінити пароль!
Скинути пароль!


Комбінований протиалергічний засіб для місцевого застосування, який містить мометазону фуроат та азеластину гідрохлорид.
ІНСТРУКЦІЯ
для медичного застосування лікарського засобу
ГЛЕНСПРЕЙ АКТИВ
(GLENSPRAY ACTIVE)
Склад:
діючі речовини: мометазону фуроат і азеластину гідрохлорид;
1 доза містить мометазону фуроату 50 мкг та азеластину гідрохлориду 140 мкг;
допоміжні речовини: целюлоза мікрокристалічна та натрію карбоксиметилцелюлоза; натрію кармелоза; глюкоза безводна; полісорбат 80; бензалконію хлорид; динатрію едетат; неотам; кислота лимонна, моногідрат; натрію цитрат; вода для ін’єкцій.
Лікарська форма. Спрей назальний, дозований, суспензія.
Основні фізико-хімічні властивості: біла або майже біла суспензія.
Фармакотерапевтична група.
Протинабрякові та інші препарати для місцевого застосування при захворюваннях порожнини носа. Кортикостероїди. Код ATХ R01A D.
Фармакологічні властивості.
Фармакодинаміка. Комбінований протинабряковий засіб для місцевого застосування, який містить мометазону фуроат та азеластину гідрохлорид.
Азеластину гідрохлорид – похідне фталазинону. Чинить пролонговану антиалергічну дію. Має виражені селективні властивості антагоніста гістамінових Н1-рецепторів. Азеластин пригнічує синтез або вивільнення хімічних медіаторів, що беруть участь у розвитку ранніх і пізніх стадій алергічних реакцій, таких як лейкотрієни, гістамін, інгібітори РАF і серотонін. Основний метаболіт азеластину – дезметилазеластин, який також є антагоністом гістамінових Н1-рецепторів.
Мометазону фуроат – синтетичний кортикостероїд для місцевого застосування, який чинить виражену протизапальну дію. Точний механізм дії кортикостероїдів при алергічному риніті поки що невідомий. Кортикостероїди демонструють широкий діапазон дії на різні клітини, а саме на гепариноцити, еозинофіли, нейтрофіли, макрофаги, лімфоцити, а також на медіатори запалення (гістамін, ейкозаноїди, лейкотрієни та цитокіни). Механізм протизапальної та протиалергічної дії мометазону фуроату в основному пов’язаний з його здатністю пригнічувати вивільнення медіаторів алергічних реакцій.
Дослідження показали, що мометазону фуроат у вигляді назального спрею 50 мкг/дозу при місцевому застосуванні знижує рівень деяких медіаторів ранньої та пізньої фази алергічної реакції, зменшує (порівняно з плацебо) рівень гістаміну та еозинофільного катіонного протеїну і знижує (порівняно з базовим значенням) кількість еозинофілів, нейтрофілів та адгезивних протеїнів епітеліальних клітин.
Фармакокінетика. Окремого фармакокінетичного дослідження назального спрею із вмістом азеластину гідрохлориду та мометазону фуроату (140 мкг/50 мкг) не проводилося.
Абсорбція
Після інтраназального застосування 2 впорскувань в кожну ніздрю назального спрею азеластину (загальна доза 548 мкг) середня пікова концентрація азеластину в плазмі (Cmax) становить 200 пг/мл, середня системна експозиція (AUC) – 5122 пг × год/мл, середній час Tmax) для досягнення Cmax становить 3 години. Системна біодоступність азеластину гідрохлориду після інтраназального застосування становить приблизно 40 %.
Суспензія мометазону фуроату при застосуванні у вигляді назального спрею має дуже низьку біодоступність (<1 %), що продемонстрував чутливий кількісний аналіз з нижньою межею кількісного визначення (LOQ) 0,25 пг/мл.
Розподіл
При внутрішньовенному та пероральному застосуванні рівноважний об’єм розподілу азеластину становить 14,5 л/кг. In vitro зв’язування з білками плазми азеластину та його активного метаболіту дезметилазеластину становить відповідно 88 % і 97 %.
In vitro зв’язування з білками плазми мометазону фуроату знаходиться у межах від 98 до 99 % при діапазоні концентрацій від 5 до 500 нг/мл.
Метаболізм
Азеластин метаболізується шляхом окислення ферментною системою цитохрому P450 до основного активного метаболіту – дезметилазеластину. Специфічні ізоформи P450, відповідальні за біотрансформацію азеластину, не були ідентифіковані. Після однократного інтраназального застосування назального спрею азеластину (загальна доза 548 мкг) середнє значення Cmax дезметилазеластину становить 23 пг/мл, AUC – 2131 пг × год/мл, середній Tmax становить 24 години. Після досягнення рівноважної концентрації азеластину при інтраназальному застосуванні плазмові концентрації дезметилазеластину знаходилися у діапазоні 20–50 % від концентрацій азеластину.
Дослідження показали, що частина дози мометазону фуроату, що проковтується і всмоктується, піддається активному метаболізму. В плазмі основних метаболітів виявлено не було. Після інкубації in vitro одним з другорядних метаболітів, який утворився, був 6β-гідроксимометазону фуроат. У мікросомах печінки людини формування метаболіту регулюється цитохромом Р450 3А4 (CYP3A4).
Виведення
Після інтраназального застосування назального спрею азеластину період напіввиведення азеластину становив 22 години, дезметилазеластину – 52 години. Приблизно 75 % пероральної дози азеластину гідрохлориду, міченого радіоактивним ізотопом, виводилося з організму з калом, причому менше 10 % – у вигляді незміненого азеластину.
Після внутрішньовенного застосування період напіввиведення мометазону фуроату становить 5,8 години. Виводиться з організму у вигляді метаболітів в основному з жовчю і в обмеженій кількості – з сечею.
Фармакокінетика у окремих груп пацієнтів.
Печінкова недостатність
Після перорального застосування азеластину печінкова недостатність не впливала на фармакокінетичні параметри.
Введення одноразової інгаляційної дози 400 мкг мометазону фуроату пацієнтам з печінковою недостатністю легкого, середнього та тяжкого ступеня лише у 1 або 2 пацієнтів з кожної групи спричинило появу пікових плазмових концентрацій мометазону фуроату (від 50 до 105 пг/мл), що визначалися. Спостережувані пікові плазмові концентрації збільшуються з ростом вираженості печінкової недостатності.
Ниркова недостатність
Дослідження перорального застосування однократних доз азеластину пацієнтам з нирковою недостатністю (кліренс креатиніну <50 мл/хв) показали підвищення Cmax і AUC на 70–75 % порівняно зі здоровими добровольцями. Час досягнення максимальної концентрації не змінився.
Вплив ниркової недостатності на фармакокінетику мометазону фуроату не досліджувався.
Вік
Вік не впливав на фармакокінетичні параметри азеластину при його пероральному застосуванні. Фармакокінетика мометазону фуроату не досліджувалася у педіатричній популяції.
Стать
У разі перорального застосування азеластину стать не впливала на його фармакокінетичні параметри. Вплив статі на фармакокінетику мометазону фуроату не досліджувався.
Клінічні характеристики.
Показання.
Сезонний алергічний риніт.
Цілорічний алергічний риніт.
Протипоказання.
Гіперчутливість до азеластину гідрохлориду, мометазону фуроату або до інших компонентів препарату.
Нелікована локальна інфекція слизової оболонки носа.
Травма носа або нещодавно перенесена операція на носі.
Взаємодія з іншими лікарськими засобами та інші види взаємодій.
Спеціальних досліджень лікарської взаємодії комбінації у фіксованих дозах азеластину гідрохлориду та мометазону фуроату у вигляді назального спрею не проводилося. Нижче наведено дані щодо окремих компонентів, які входять до складу препарату. Оскільки мометазон і азеластин впливають на різні види рецепторів, лікарська взаємодія при застосуванні цієї комбінації не очікується.
Азеластину гідрохлорид
Депресанти центральної нервової системи
При одночасному застосуванні азеластину з алкоголем або з іншими депресантами центральної нервової системи можливе зниження концентрації уваги і погіршення функцій центральної нервової системи.
Еритроміцин і кетоконазол
Оцінка ЕКГ пацієнтів, які одночасно застосовували перорально азеластину гідрохлорид і еритроміцин або кетоконазол, показує, що клінічно значущий вплив на QT-інтервал (або величину QTc) відсутній. Пероральне застосування еритроміцину у дозі 500 мг 3 рази на день протягом 7 днів не впливало на фармакокінетику азеластину та величину QTc. Кетоконазол при застосуванні у дозі 200 мг 2 рази на день протягом 7 днів перешкоджав вимірюванню плазмових концентрацій азеластину методом аналітичної високоефективної рідинної хроматографії (ВЕРХ); однак впливу на величину QTc не спостерігалось.
Циметидин
Циметидин у дозі 400 мг двічі на день при одночасному пероральному застосуванні з азеластину гідрохлоридом у дозі 4 мг двічі на день підвищує середнє значення Cmax і AUC останнього приблизно на 65 %.
Мометазону фуроат
Інгібітори цитохрому P450 3A4
Кетоконазол
Мометазону фуроат головним чином метаболізується в печінці. Дослідження in vitro підтвердили першорядну роль цитохрому CYP3A4 у метаболізмі цієї сполуки. Одночасне застосування з кетоконазолом, потужним інгібітором CYP3A4, може збільшити плазмові концентрації мометазону фуроату.
Ритонавір
Ритонавір як інгібітор протеази може пригнічувати метаболізм мометазону фуроату при одночасному застосуванні, що призводить до збільшення системного впливу останнього та збільшення ризику виникнення побічних ефектів.
Лоратадин
Клінічні дослідження лікарської взаємодії були проведені з лоратадином. Взаємодії не спостерігалося.
Особливості застосування.
Азеластину гідрохлорид
У клінічних випробуваннях повідомлялось про появу сонливості у деяких пацієнтів, які застосовували азеластину гідрохлорид у вигляді назального спрею. Під час лікування препаратом пацієнтам слід утримуватись від роботи, що вимагає підвищеної концентрації уваги та швидкості реакцій.
Слід уникати одночасного застосування назального спрею азеластину з алкоголем або з іншими депресантами центральної нервової системи через можливе пригнічення функцій центральної нервової системи.
Мометазону фуроат
Локальний вплив на ніс
Носова кровотеча
У клінічних дослідженнях носова кровотеча спостерігалася частіше у пацієнтів з алергічним ринітом, які отримували мометазону фуроат у вигляді назального спрею, ніж ті, хто отримував плацебо.
Грибкова інфекція
У клінічних дослідженнях після введення мометазону фуроату у вигляді назального спрею 50 мкг/дозу в окремих випадках спостерігався розвиток локалізованої грибкової інфекції носа і глотки (Candida albicans). У разі виникнення грибкової інфекції застосування препарату слід припинити та, якщо необхідно, розпочати відповідне лікування.
Перфорація носової перегородки
Поодинокі випадки перфорації носової перегородки спостерігалися у пацієнтів після застосування інтраназальних кортикостероїдів, включаючи мометазону фуроат. Як і впродовж будь-якого довготривалого місцевого лікування носової порожнини, пацієнтам, які застосовують назальний спрей з мометазону фуроатом протягом кількох місяців і довше, необхідно періодично проходити огляд щодо можливих змін слизової оболонки носа.
Порушення загоєння ран
Через гальмівний вплив кортикостероїдів на загоєння ран пацієнти, які нещодавно перенесли виразки носової перегородки, хірургічне втручання на носі або травму носа, не повинні застосовувати назальні кортикостероїди до повного одужання.
Порушення зору
При застосуванні кортикостероїдів системної та місцевої дії (включаючи інтраназальне, інгаляційне та внутрішньоочне введення) можуть виникнути порушення зору. Якщо виникають такі симптоми, як нечіткість зору або інші порушення зору, пацієнту слід пройти обстеження у офтальмолога для оцінки можливих причин порушення зору, які можуть включати катаракту, глаукому або такі рідкісні захворювання, як центральна серозна хоріоретинопатія, про що повідомлялося після заcтосування кортикостероїдів системної та місцевої дії.
Реакції гіперчутливості
Реакції гіперчутливості, включаючи випадки свистячого дихання, можуть виникати після інтраназального застосування мометазону фуроату. У такому разі терапію препаратом слід припинити.
Імуносупресія
Пацієнти, які лікуються препаратами, що пригнічують імунну систему, більш сприйнятливі до інфекцій, ніж здорові люди. Наприклад, вітрянка і кір мають більш тяжкий перебіг у дітей та дорослих зі зниженим імунітетом, які застосовують кортикостероїди. Такі пацієнти потребують особливої уваги та застосування противірусних препаратів або вакцинації. Вплив дози, способу і тривалості застосування кортикостероїдів на ризик розвитку генералізованої інфекції поки що невідомий.
Назальний спрей мометазону фуроату слід застосовувати з обережністю або не застосовувати зовсім хворим з активною або латентною туберкульозною інфекцією респіраторного тракту, а також при нелікованій грибковій, бактеріальній, системній вірусній інфекції або при інфекції herpes simplex з ураженням очей.
Вплив на гіпоталамо-гіпофізарно-наднирковозалозну систему
Гіперадренокортицизм і адренальна супресія
При тривалому застосуванні інтраназальних кортикостероїдів, особливо у високих дозах, можуть відмічатися системні ефекти, такі як гіперадренокортицизм і адренальна супресія. Важливо, щоб при досягненні терапевтичного ефекту доза інтраназальних кортикостероїдів була знижена до мінімальної ефективної дози, яка контролює перебіг захворювання, щоб уникнути розвитку системних побічних ефектів.
У разі появи ознак розвитку небажаного системного впливу лікування назальним спреєм з мометазону фуроатом слід поступово припинити.
Вплив на динаміку росту у дітей
Кортикостероїди, включаючи мометазону фуроат, можуть призвести до затримки росту у дітей. Рекомендується регулярно стежити за динамікою росту дітей, які лікуються інтраназальними кортикостероїдами протягом тривалого часу.
Щоб мінімізувати системні ефекти назальних кортикостероїдів, зокрема мометазону фуроату, слід титрувати дозу для кожного пацієнта до найнижчої дози, яка ефективно контролює симптоми.
Гленспрей Актив містить бензалконію хлорид, який може спричинити подразнення слизової оболонки носа і бронхоспазм.
Слід пам’ятати, що кортикостероїди мають особливо потужний діабетогенний ефект і можуть призвести до збільшення печінкового глюконеогенезу та зниження поглинання глюкози периферичними тканинами та до гіперглікемії.
Застосування пацієнтам літнього віку.
Клінічні дані щодо безпеки застосування лікарського засобу пацієнтам літнього віку відсутні.
Застосування у період вагітності або годування груддю.
Спеціальних досліджень дії препарату у період вагітності або годування груддю не проводилося.
Застосування у період вагітності.
Азеластину гідрохлорид. Адекватних і контрольованих клінічних випробувань за участю вагітних жінок не проводилося. У дослідах на тваринах азеластину гідрохлорид спричиняв ембріотоксичність.
Мометазону фуроат. Адекватних і контрольованих клінічних випробувань за участю вагітних жінок не проводилося.
Слід звернути увагу на те, що завдяки природному збільшенню продукування кортикостероїдів під час вагітності більшість жінок потребує менших доз екзогенних кортикостероїдів, а багатьом з них не потрібне лікування кортикостероїдами у період вагітності.
Мометазон мінімально всмоктується системно після назального застосування, і не очікується, що застосування лікарського засобу матір’ю матиме вплив на плід. Наявних даних обсерваційних досліджень застосування мометазону фуроату вагітними жінками недостатньо для оцінки ризику серйозних вроджених дефектів, викидня або інших несприятливих наслідків для матері чи плода. У репродуктивних дослідженнях на вагітних мишах, щурах або кроликах мометазону фуроат (підшкірне, місцеве нашкірне та пероральне застосування) викликав збільшення вад розвитку плода і зниження виживання та росту плода після введення доз, які в ⅓–8 разів перевищували максимальну рекомендовану дозу для людини у перерахунку на мкг/м2 або AUC. Однак досвід застосування пероральних кортикостероїдів показує, що гризуни більш схильні до тератогенних ефектів від впливу кортикостероїдів, ніж люди.
Розрахунковий фоновий ризик серйозних вроджених дефектів і викидня для зазначеної популяції невідомий. Усі вагітності мають фоновий ризик вроджених вад, втрати або інших несприятливих наслідків. У загальній популяції США оцінений ризик серйозних вроджених дефектів і викидня під час клінічно визнаних вагітностей становить 2–4 % і 15–20 % відповідно.
У дослідженні ембріофетального розвитку на вагітних мишах, які отримували дозу протягом періоду органогенезу, мометазону фуроат викликав розщеплення піднебіння в дозі, меншій за максимальну рекомендовану добову інтраназальну дозу (МРДІД) (у перерахунку на мкг/м2, підшкірні дози для матері 60 мкг/кг і вище) і зниження виживаності плода в дозі, меншій приблизно в 2 рази за МРДІД (у перерахунку на мкг/м2, підшкірна доза для матері 180 мкг/кг). Токсичність не спостерігалася при дозі, яка була менше, ніж МРДІД (у перерахунку на мкг/м2, місцеві нашкірні дози для матері 20 мкг/кг і вище).
Застосування у період годування груддю.
Азеластину гідрохлорид. Невідомо, чи виділяється азеластину гідрохлорид у грудне молоко людини.
Мометазону фуроат. Невідомо, чи виділяється мометазону фуроат у грудне молоко людини.
Препарат мінімально системно всмоктується у матері після назального застосування, і не очікується впливу мометазону на немовля через материнське молоко. Однак слід враховувати переваги грудного вигодовування для розвитку та здоров’я немовляти і клінічну потребу матері в мометазоні, а також будь-який потенційний несприятливий вплив мометазону фуроату або основного захворювання матері на дитину.
Здатність впливати на швидкість реакції при керуванні автотранспортом або іншими механізмами.
Спеціальних досліджень впливу препарату на здатність керувати транспортними засобами та іншими механізмами не проводилося.
Оскільки були повідомлення про появу сонливості у деяких пацієнтів, які в ході клінічних досліджень застосовували азеластину гідрохлорид в лікарській формі назального спрею, під час лікування препаратом пацієнтам слід утримуватись від роботи, що вимагає підвищеної концентрації уваги та швидкості реакцій.
Спосіб застосування та дози.
Препарат призначений тільки для інтраназального застосування.
Дорослі і діти віком від 12 років. Рекомендована доза становить 1 впорскування в кожну ніздрю 2 рази на добу.
Пацієнти з порушенням функції нирок. Корекція дози не потрібна пацієнтам з нирковою недостатністю легкого ступеня (кліренс креатиніну > 79 мл/хв). Пацієнтам з помірною та тяжкою нирковою недостатністю (кліренс креатиніну < 79 мл/хв – > 10 мл/хв) препарат слід застосовувати з обережністю та під суворим наглядом лікаря.
Пацієнти з печінковою недостатністю. Корекція дози не потрібна.
Літні пацієнти. Не спостерігалося відмінностей у безпеці та/або ефективності у літніх пацієнтів порівняно з молодшими дорослими пацієнтами.
Застосування назального спрею
Перед кожним застосуванням флакон необхідно обережно струснути протягом 5 секунд. Після цього зняти захисний ковпачок. Перед першим використанням флакона слід натиснути на дозуючий пристрій 6 разів поспіль. Якщо назальний спрей не використовувався більше 7 днів, перед використанням потрібно повторно натиснути на дозуючий насос-розпилювач 6 разів поспіль.
Перед кожним застосуванням слід ретельно очистити ніс від слизу. Після очищення носа суспензію впорскують в кожну ніздрю, при цьому голову слід утримувати трохи нахиленою вниз. Після застосування наконечник розпилювача потрібно протерти і накрити захисним ковпачком.
У разі закупорення насоса-розпилювача його потрібно очистити, як описано нижче.
Не намагайтеся прочистити розпилювач голкою або іншим гострим предметом — Ви можете його пошкодити і отримати неправильну дозу лікарського засобу.
Щоб очистити розпилювач, зніміть ковпачок (рисунок 1).
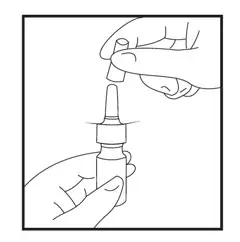
Рисунок 1
Обережно потягніть вгору білий розпилювач для того, щоб його вийняти.
Помістіть розпилювач та пилозахисний ковпачок у теплу воду на декілька хвилин, потім ретельно промийте наконечник розпилювача та пилозахисний ковпачок у теплій воді і, нарешті, промийте чистою проточною водою (рисунок 2).
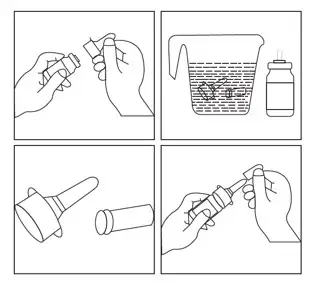
Рисунок 2
Коли розпилювач висохне, встановіть його на місце, переконавшись у тому, що стрижень насоса знову вставлений в центральний отвір розпилювача (рисунок 3).
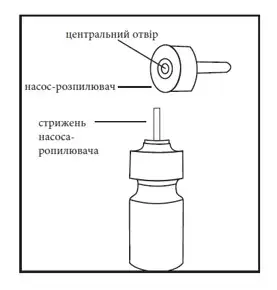
Рисунок 3
Підготуйте розпилювач до подальшого використання, натиснувши з боків верхньої частини розпилювача вказівним і середнім пальцями, одночасно утримуючи основу флакона великим пальцем. Натисніть і відпустіть насос-розпилювач 2 рази або натискайте до того часу, поки не з’явиться струмінь дрібнодисперсного аерозолю (повторіть описану вище процедуру промивання, якщо аерозоль не з’являється). Не розпилюйте спрей в очі. Тепер насос-розпилювач готовий до використання.
Насос-розпилювач може зберігатися без використання до 1 тижня без необхідності повторного підготовчого розпилення спрею в повітря. Якщо насос-розпилювач не використовується протягом більш ніж 1 тижня, підготуйте його до використання шляхом натискання на розпилювач 2 рази або до того часу, поки не з’явиться струмінь дрібнодисперсного аерозолю (рисунок 4).
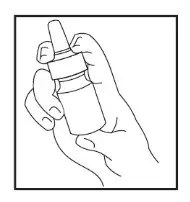
Рисунок 4
Після використання надіньте на розпилювач захисний ковпачок (рисунок 5).
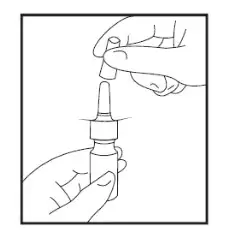
Рисунок 5
Діти.
Немає достатнього клінічного досвіду застосування препарату дітям віком до 12 років, тому його не слід застосовувати пацієнтам цієї вікової категорії.
Встановлено безпеку та ефективність мометазону фуроату для профілактики назальних симптомів сезонного алергічного риніту у педіатричних пацієнтів віком від 12 років. Можливість застосування мометазону фуроату за цим показанням підтверджено у контрольованих дослідженнях за участю дорослих та дітей віком від 12 років.
Вплив на ріст
Контрольовані клінічні дослідження показали, що назальні кортикостероїди можуть спричиняти уповільнення росту у дітей. Цей ефект спостерігався за відсутності лабораторних доказів пригнічення осі «гіпоталамус — гіпофіз — наднирники» (ГГН), що свідчить про те, що швидкість росту є більш чутливим показником системного впливу кортикостероїдів у педіатричних пацієнтів, ніж деякі тести функції осі ГГН, які зазвичай застосовуються. Довгострокові наслідки цього зниження швидкості росту, пов’язані з назальними кортикостероїдами, включаючи вплив на кінцевий зріст дорослої людини, невідомі. Потенціал «наздогінного» зростання після припинення лікування назальними кортикостероїдами не був належним чином вивчений. Зростання дітей, які отримують назальні кортикостероїди, включаючи мометазону фуроат, слід регулярно контролювати (наприклад, за допомогою стадіометрії). Потенційний вплив тривалого лікування на ріст слід зіставляти з отриманими клінічними перевагами та наявністю безпечних і ефективних альтернатив лікування некортикостероїдами. Щоб звести до мінімуму системні ефекти назальних кортикостероїдів, включаючи мометазону фуроат, кожному пацієнту слід підбирати найменшу ефективну дозу.
Передозування.
Повідомлень щодо передозування препаратом Гленспрей Актив немає.
У разі гострого передозування можливі порушення з боку центральної нервової системи (сонливість, запаморочення). Пероральне одноразове застосування азеластину гідрохлориду у дозі до 16 мг під час клінічних досліджень не призвело до підвищення частоти серйозних небажаних ефектів. Лікування симптоматичне. Антидот невідомий.
Немає повідомлень про випадки гострого або хронічного передозування мометазону фуроатом у вигляді назального спрею. Повідомлялося про застосування одноразових інтраназальних доз до 4 мг і пероральних інгаляційних доз до 8 мг добровольцям без будь-яких побічних ефектів.
Хронічне передозування будь-яким кортикостероїдом може призвести до появи симптомів гіперкортицизму.
Побічні реакції.
У ході клінічного дослідження побічні ефекти, пов’язані із застосуванням назального спрею із вмістом азеластину гідрохлориду та мометазону фуроату, були зареєстровані у 11 пацієнтів із 282, які брали участь у дослідженні. Всього було зареєстровано 18 випадків небажаних реакцій, пов’язаних з лікуванням комбінацією азеластину і мометазону. Найбільш поширеними побічними реакціями були головний біль і дисгевзія. Іншими побічними реакціями були сонливість, млявість, нудота, диспепсія і чхання. Більшість побічних ефектів були легкого ступеня тяжкості, і в ході дослідження не було повідомлень про серйозні небажані реакції.
Нижче наведено побічні реакції, які спостерігалися при застосуванні окремих компонентів препарату.
Назальний спрей азеластину гідрохлориду
Часто (1 – 10 %): специфічний гіркий смак може з’явитися після застосування спрею (найчастіше через неправильний спосіб застосування, а саме коли голова занадто відхилена назад під час впорскування препарату), що в окремих випадках може призвести до нудоти.
Нечасто (0,1 – 1 %): тимчасове подразнення запаленої слизової оболонки носа може виникнути разом з такими симптомами, як печіння, свербіж, чхання і носові кровотечі.
У дуже рідких випадках (< 0,01 %) повідомлялося про реакції гіперчутливості (висипання, свербіж, кропив’янка).
Досвід післяреєстраційного застосування
Побічні реакції, виявлені під час постмаркетингового застосування назального спрею азеластину: біль у животі, печіння в носі, нудота, солодкий присмак, подразнення горла, анафілактоїдні реакції, подразнення в місці застосування, фібриляція передсердь, порушення зору (нечіткість зору, катаракта, глаукома, центральна серозна хоріоретинопатія (див. розділ «Особливості застосування»)), біль у грудях, сплутаність свідомості, запаморочення, задишка, набряк обличчя, гіпертензія, мимовільні скорочення м’язів, нервозність, прискорене серцебиття, парестезії, паросмія, пароксизмальне чхання, свербіж, висипання, порушення або втрата нюху і/або смаку, тахікардія, імунологічна толерантність, затримка сечі, ксерофтальмія. Оскільки вказані реакції стосуються популяції невизначеної чисельності, не завжди можна достовірно оцінити їхню частоту або встановити причинно-наслідковий зв’язок із застосуванням препарату.
Назальний спрей мометазону фуроату
Респіраторні, торакальні та медіастинальні розлади: носові кровотечі, фарингіт, печіння або подразнення в носі, носові виразки – часто (1 – 10 %).
Загальні порушення та місцеві реакції: головний біль – часто (1 – 10 %).
Носові кровотечі були в основному легкого ступеня вираженості і не потребували втручання лікаря.
У дітей найчастіше спостерігалися носові кровотечі, головний біль, подразнення слизової оболонки носа, чхання.
Системні побічні ефекти під час лікування назальними кортикостероїдами можуть виникати при застосуванні високих доз протягом тривалого часу.
Досвід післяреєстраційного застосування
Побічні реакції, виявлені під час постмаркетингового застосування назального спрею мометазону фуроату: печіння і подразнення в носі, анафілаксія та ангіоневротичний набряк, порушення смаку та нюху і перфорація носової перегородки.
Клінічно значущі побічні реакції, які описані в інших розділах:
Носова кровотеча, виразки, інфекція Candida albicans, порушення загоєння ран (див. розділ «Особливості застосування»)
Глаукома та катаракта (див. розділ «Особливості застосування»)
Імуносупресія та ризик інфекцій (див. розділ «Особливості застосування»)
Гіперкортицизм і пригнічення надниркових залоз, включаючи уповільнення росту (див. розділи «Особливості застосування» та «Діти»).
Досвід клінічних випробувань
Оскільки клінічні випробування проводяться в різних умовах, частоту побічних реакцій, що спостерігаються під час клінічних випробувань лікарського засобу, неможливо безпосередньо порівняти з частотою в клінічних випробуваннях іншого лікарського засобу, і вона може не відображати частоту, що спостерігається на практиці.
Алергічний риніт: дорослі та діти віком від 12 років
У контрольованих американських і міжнародних клінічних дослідженнях загалом 3210 дорослих і дітей віком від 12 років з алергічним ринітом отримували лікування мометазону фуроатом назально у дозах від 50 до 800 мкг/добу. Більшість пацієнтів (n = 2103) отримували 200 мкг/добу. Загалом 350 дорослих і дітей віком від 12 років лікувалися протягом одного року або довше. Побічні реакції істотно не відрізнялися залежно від віку, статі чи раси. Чотири відсотки або менше пацієнтів у клінічних випробуваннях припинили лікування через побічні ефекти, і частота припинення лікування була однаковою для лікарського засобу й активних аналогів.
Усі побічні реакції (незалежно від зв’язку з лікуванням), про які повідомили щонайменше 5 % дорослих та дітей віком від 12 років, що отримували мометазону фуроат назально у дозі 200 мкг/день, спостерігалися частіше при застосуванні мометазону фуроату, ніж плацебо.
Дорослі та діти віком від 12 років: побічні реакції за результатами контрольованих клінічних досліджень при сезонному алергічному та цілорічному алергічному риніті (відсоток пацієнтів, які повідомили про це).
Інші побічні реакції, що виникали у ≥2 — <5 % дорослих і дітей віком від 12 років, які отримували мометазону фуроат назально 200 мкг/добу (незалежно від зв’язку з лікуванням), і частіше, ніж у групі плацебо: артралгія, астма, бронхіт, біль у грудях, кон’юнктивіт, діарея, диспепсія, біль у вусі, грипоподібні симптоми, міалгія, нудота та риніт.
Застосування назального спрею із вмістом азеластину гідрохлориду та мометазону фуроату у пацієнтів може призвести до підвищення рівня АЛТ, АСТ.
Застосування препарату Гленспрей Актив може призвести до розвитку порушення з боку нирок та сечовидільної системи (гематурія).
Кортикостероїди стимулюють секрецію кислоти та пепсину, що може призвести до розвитку гастриту та гіперхлоргідрії.
Термін придатності.
2 роки.
Умови зберігання.
Зберігати в захищеному від світла місці при температурі не вище 25 °C. Не заморожувати. Зберігати у недоступному для дітей місці.
Упаковка.
По 75 або 150 доз у поліетиленовому флаконі. По 1 флакону з дозуючим насосом-розпилювачем, закритим ковпачком, у картонній коробці.
Категорія відпуску.
За рецептом.
Виробник.
Гленмарк Фармасьютикалз Лтд. / Glenmark Pharmaceuticals Ltd.
Місцезнаходження виробника та його адреса місця провадження діяльності.
Блок ІІІ, село Кішанпура, Бадді-Налагарх Роуд, техсіл Бадді, р-н Солан, Х.П. 173 205, Індія /
Unit III, Village Kishanpura, Baddi-Nalagarh Road, Tehsil Baddi, Distt. Solan (H.P.) 173 205, India.
Джерело: Державний реєстр лікарських засобів України (drlz.com.ua) http://www.drlz.com.ua/ibp/lz_www.nsf/id/83EB30F07551250AC2258B0300267549/$file/UA145500101_28D9.mht; дата останнього звернення: 10.06.2024. У випадках виявлення розбіжності версії на даній сторінці з версією за постійним посиланням в Державному реєстрі лікарських засобів України (Інформаційний фонд), слід користуватися офіційною версією в Держреєстрі.
Інформація про лікарський засіб, призначена для медичних і фармацевтичних працівників. Перед призначенням ознайомтесь з інструкцією для медичного застосування лікарського засобу.
За додатковою інформацією звертайтесь за адресою: ТОВ «Др. Редді'с Лабораторіз» Столичне шосе, 103, оф. 11-А, м. Київ, Україна, 03131, тел. +380444923173
1GleA-04-06-2024-OTC-7.1.
Коментарі (0)