Змінити пароль!
Скинути пароль!


Один із очікуваних наслідків постаріння населення - це збільшення тягаря вікових когнітивних порушень.
Один із очікуваних наслідків постаріння населення - це збільшення тягаря вікових когнітивних порушень. Поки не існує ефективних фармацевтичних засобів лікування, вивчаються різні стратегії профілактики. Існує чимало доказів того, як певні поживні речовини та біоактивні сполуки можуть вплинути на когнітивні функції [1]. Холін є одним із найважливіших нутрієнтів для розвитку і функціонування мозку. Метаболіти холіну ацетилхолін та фосфатидилхолін сприяють належній сигналізації для нормальної холінергічної нейротрансмісії та структурної цілісності клітинних мембран [2]. Збагачення раціону холіном асоціюється з покращенням когнітивних показників у літніх людей [3, 4]. Одним із способів збільшення харчового надходження холіну є прийом дієтичних добавок, які містять цитиколін.
Цитиколін - природний мононуклеотид, що складається з цитозину, рибози, пірофосфату та холіну. Він виробляється в організмі як проміжний продукт в реакціях біосинтезу фосфатидилхоліну та сфінгомієліну [5]. Нейропротекторні дії цитиколіну включають активізацію біосинтезу структурних фосфоліпідів у мембранах нейронів, посилення метаболізму мозку, підвищення рівнів норадреналіну та дофаміну в центральній нервовій системі, запобігання втраті кардіоліпіну (критично важливого внутрішнього мітохондріального фосфоліпіду, збагаченого ненасиченими жирними кислотами), та захист клітинних мембран шляхом прискорення оновлення фосфоліпідів [6].
Скринінгове обстеження пройшли 426 осіб, а 100 учасників були рандомізовані. Між групами цитиколіну та плацебо не було статистично значущих відмінностей в базових демографічних та клінічних характеристиках. Cередній вік в групах цитиколіну і плацебо становив 65,5 і 63,2 року відповідно. В обох групах переважали жінки (68,6 і 61,2% відповідно). Початкові оцінки MMSE становили 27,6 і 27,8 бали.
Дослідження повністю завершили 99 учасників. Комплаєнс протягом 12-ти тижневого періоду становив 99,2 ± 0,5% для 99 учасників, які завершили дослідження.
Дизайн та учасники дослідження
Рандомізоване, подвійне сліпе, плацебо-контрольоване дослідження проводилося в Biofortis Inc. (Аддісон, Іллінойс) у період з січня 2018 року по грудень 2018 року (внесено до реєстру ClinicalTrials.gov з ідентифікатором NCT03369925).
Здорових чоловіків та жінок відбирали за критеріями вікового порушення пам’яті, запропонованими Національним інститутом охорони здоров’я США (19): вік 50–85 років, оцінка ≥24 за міні-тестом психічного стану (MMSE); ≥ 85 за коротким тестом інтелекту Кауфмана (друге видання); ≤5 за шкалою геріатричної депресії та 4, 3 або 2 за тестом просторової орієнтації.
Прийняті учасники були випадковим чином розподілені в співвідношенні 1:1 в групи перорального споживання дієтичної добавки цитиколіну (500 мг/добу, 2 капсули за сніданком) або ідентичних капсул плацебо у подвійному сліпому режимі протягом 12 тижнів.
Процедури дослідження
Дослідження включало 1 скринінговий візит, 2 тестові візити (тиждень 0 та тиждень 12) та 1 візит, на якому визначали комплаєнс за відсотком прийнятих капсул (тиждень 6). Щоб мінімізувати вплив змін способу життя на результати, учасникам було запропоновано дотримуватись звичної дієти, режиму активності та тривалості сну протягом усього дослідження, а будь-які серйозні зміни/стресові події в житті, які могли вплинути на когнітивні функції, були відстежені та задокументовані. На початку (тиждень 0) та наприкінці дослідження (тиждень 12) учасники прибували до клініки натще, отримували стандартний сніданок та виконували тести на когнітивні функції.
Когнітивні тести
Когнітивні показники оцінювали за допомогою набору комп'ютерних тестів Cambridge Brain Sciences (Торонто, Онтаріо, Канада). Це загальнодоступна тестова батарея, валідована Радою медичних досліджень та підрозділом наук про мозок (Кембридж, Великобританія) [9, 10]. Проводили оцінювання робочої пам'яті (завдання «мавп’яча драбина»), короткочасної просторової пам'яті (тест відтворення просторового розташування), короткочасної словесної пам'яті (тест відтворення числового ряду), епізодичної пам'яті (тест парних асоціацій), вибіркової уваги (тести зіставлення фігур за ознаками і порівняння багатокутників) та постійної уваги (тест підтримання уваги до відповіді).
Первинною кінцевою точкою дослідження була зміна балів тесту просторової пам’яті, обчислена як різниця вихідної оцінки та оцінки на 12-му тижні для кожного учасника. Вторинні кінцеві точки включали зміни в тестових балах для решти 6 когнітивних завдань.
Усі статистичні аналізи були проведені за допомогою SAS для Windows (версія 9.4, Кері, Північна Кароліна) для сукупності рандомізованих пацієнтів, які отримали принаймні одну дозу досліджуваного препарату (популяція ITT).
Жоден з небажаних ефектів не був серйозним. Вісім легких побічних реакцій були визнані «можливо» пов'язаними з одним із досліджуваних продуктів (2 у групі плацебо та 6 у групі цитиколіну). Усі 6 небажаних реакцій у групі цитиколіну (підвищений апетит, збільшення маси тіла, підвищена флатуленція (2 випадки), головний біль та посилення відрижки) були легкими та тимчасовими, і не були несподіваними на підставі попередніх досліджень з препаратом
Кокрейнівський систематичний огляд підтвердив сприятливий вплив споживання цитиколіну на функції пам’яті та поведінку у осіб з широким спектром нейропсихіатричних порушень, таких як легкі та помірні судинні когнітивні порушення, судинна деменція або стареча деменція [7]. До недавна залишалося відкритим питання, як впливає регулярний пероральний прийом цитиколіну на когнітивні функції у здорових літніх людей із віковим погіршенням пам’яті. Метою дослідження групи науковців з Японії та США (E. Nakazaki та співавт. [8]) було дослідити вплив дієтичної добавки цитиколіну у дозі 500 мг/добу на пам’ять у здорових людей похилого віку з погіршенням пам’яті.
Динаміка когнітивних функцій
Результати тестів когнітивних функцій на вихідному візиті та 12-му тижні наведені в Таблиці 1. В групі цитиколіну, на відміну від групи плацебо, було відзначено статистично значуще покращення просторової пам’яті, вибіркової уваги в тесті зіставлення фігур за ознаками, а також загальної оцінки пам'яті по відношенню до вихідних рівнів. Міжгруповий аналіз показав статистично значущі відмінності (P <0,00625) за результатами тесту парних асоціацій та загальної оцінки пам’яті, тобто група цитиколіну продемонструвала більші покращення у цих тестах порівняно з групою плацебо (рисунки 1, 2) . У решті тестів не було виявлено додаткових статистично значущих когнітивних ефектів за результатами множинних порівнянь з поправкою Бонферроні.
Таблиця 1. Результати когнітивних тестів в групах цитиколіну та плацебо в популяції ІТТ, 0-й та 12-й тижні.
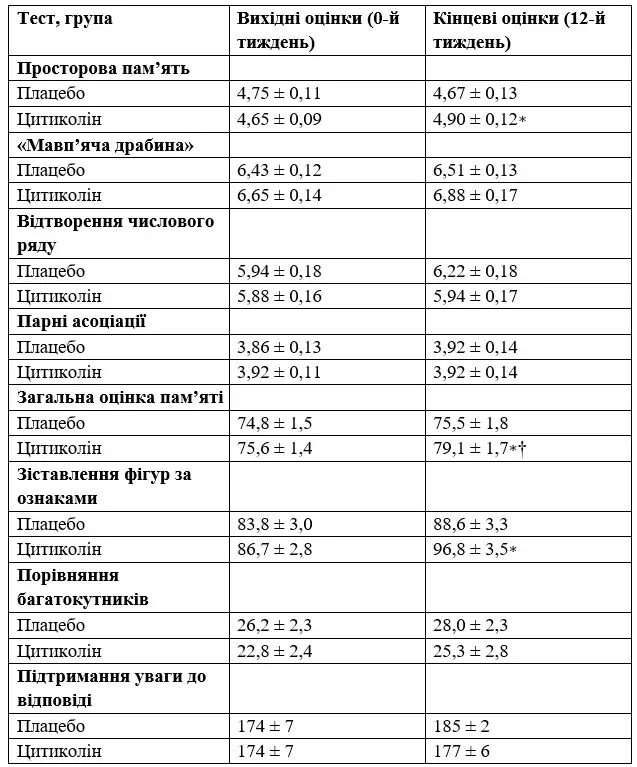
Примітки: Значення в таблиці представлені як середні значення ± SEM тестового балу. Підвищення загальної оцінки пам’яті та всіх балів кожного окремого когнітивного тесту свідчить про поліпшення.
∗ P <0,05 різниця в групі (вихідний рівень порівняно з кінцем дослідження) за даними парного t-тесту.
† P <0,05 різниця між групами щодо необроблених результатів, проаналізовано за допомогою ANCOVA з корекцією Бонферроні для множинних порівнянь. Необроблені результати обчислювалися як різниця в балах на вихідному рівні та наприкінці тестового періоду для кожного учасника.
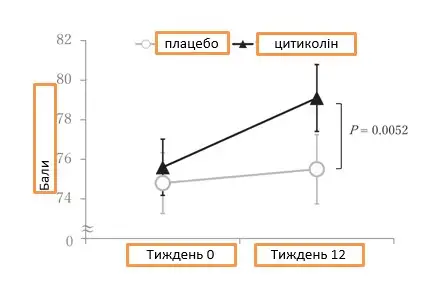
РИСУНОК 1. Загальні оцінки пам’яті до початку дослідження та після 12 тижнів прийому цитиколіну або плацебо. Наведені дані є некоригованими середніми ± SEM для кожної тестової групи. Збільшення балів свідчить про поліпшення. Значення P вказує на статистично значущу різницю між групами щодо необроблених результатів тестів, отриману в аналізі ANCOVA з корекцією Бонферроні для множинних порівнянь. Необроблені результати обчислювалися як різниця в балах на вихідному рівні та наприкінці тестового періоду для кожного учасника.
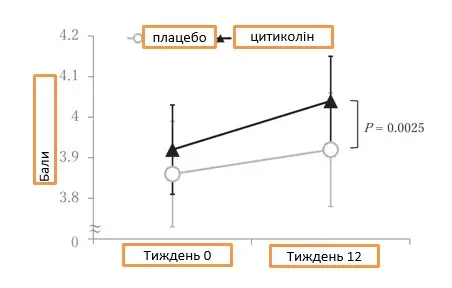
РИСУНОК 2 Результати тесту на парні асоціації до початку дослідження та після 12 тижнів прийому цитиколіну або плацебо. Наведені дані є некоригованими середніми ± SEM для кожної тестової групи. Збільшення балів свідчить про поліпшення. Значення P вказує на статистично значущу різницю між групами щодо необроблених результатів тесту, отриману в аналізі ANCOVA з корекцією Бонферроні для множинних порівнянь. Необроблені результати обчислювалися як різниця в балах на вихідному рівні та наприкінці тестового періоду для кожного учасника.
Це перше рандомізоване, подвійне сліпе, плацебо-контрольоване дослідження в паралельних групах для оцінки впливу на показники пам’яті та інші когнітивні домени тривалого (12 тижнів) прийому дієтичної добавки цитиколіну в дозі 500 мг/добу здоровими літніми особами. У порівнянні з групою плацебо учасники, які приймали цитиколін, продемонстрували значне поліпшення епізодичної пам’яті, оціненої за допомогою тесту парних асоціацій, та загальної оцінки пам’яті. Цей результат узгоджуються з попередніми дослідженнями, які продемонстрували корисний вплив цитиколіну на пам’ять [11, 12].
Епізодична пам’ять – це здатність запам’ятовувати та згадувати певні події в поєднанні з контекстом, в якому вони відбувалися, наприклад, ідентифікувати, коли і де зустрічався об’єкт [13]. Зниження епізодичної пам’яті часто проявляється як неможливість згадати минулі події або отримати уроки з минулого досвіду, що може призвести до повторних помилок. Епізодична пам'ять більш вразлива при старінні, ніж інші види пам'яті [14]. Дослідження Nakazaki та колег є першим, що продемонструвало сприятливий вплив додавання цитиколіну до раціону на збереження та/або поліпшення епізодичної пам’яті, яка погіршується з віком.
На додачу до статистично значущого поліпшення в тесті парних асоціацій, дослідники спостерігали тенденцію до поліпшення виконання тесту на просторову пам’ять в групі цитиколіну. Раніше Оуен повідомив про активацію середньо-вентролатеральної лобної кори під час виконання завдань з просторової орієнтації та парних асоціацій [9]. В інших дослідженнях за участі людей було показано, що цитиколін покращує біоенергетику лобних часток мозку і стимулює оновлення фосфоліпідних мембран [15]. Вікове зниження когнітивних здібностей, особливо пов'язане з функціями лобної частки, було продемонстровано у людей [16, 17]. У сукупності ці дані свідчать про те, що активація серединної вентролатеральної лобної кори є можливим механізмом дії, за допомогою якого цитиколін покращує когнітивні функції.
Nakazaki з колегами також спостерігали поліпшення вибіркової уваги, оцінюваної за допомогою тесту зіставлення фігур за ознаками, у групі цитиколіну порівняно з вихідним показником; хоча суттєвої різниці між групами не було. Ця тенденція разом із позитивним ефектом, повідомленим у попередньому дослідженні [18], свідчить про позитивний вплив цитиколіну на увагу, що заслуговує на подальше вивчення.
Клінічне дослідження за участі здорових добровольців, які споживали 500 мг/добу цитиколіну протягом 6 тижнів, продемонструвало підвищений рівень фосфодіефірів - неінвазивного біомаркера синтезу фосфоліпідів у мозку. Таким чином, здатність цитиколіну збільшувати синтез фосфатидилхоліну в мозку людей вважається доведеною [19]. Рівні фосфатидилхоліну в плазмі позитивно асоціюються з когнітивною гнучкістю у здорових літніх людей. Нижня префронтальна кора опосередковує зв'язок між фосфатидилхоліном у плазмі та когнітивною гнучкістю [20]. Збільшення рівня фосфодіефірів корелювало з покращенням виконання Каліфорнійського тесту вербального навчання у здорових літніх людей [19]. У сукупності ці результати свідчать про те, що цитиколін може уповільнити або запобігти порушенню пам’яті з віком, впливаючи на специфічні структури в мозку.
У підсумку, споживання дієтичної добавки цитиколіну впродовж 3 місяців покращувало загальну продуктивність пам’яті, особливо епізодичну пам’ять у здорових чоловіків та жінок з віковим погіршенням пам’яті. Регулярне споживання цитиколіну може бути безпечним і потенційно корисним проти втрати пам’яті через старіння.
1. Prince M, Albanese E, Guerchet M, Prina M. World Alzheimer Report 2014: dementia and risk reduction. London: Alzheimer’s Disease International (ADI); 2014.
2. Zeisel SH. Choline: critical role during fetal development and dietary requirements in adults. Annu Rev Nutr 2006;26:229–50.
3. Poly C, Massaro JM, Seshadri S, Wolf PA, Cho EY, Krall E, Jacques PF, Au R. The relation of dietary choline to cognitive performance and white-matter hyperintensity in the Framingham Offspring Cohort. Am J Clin Nutr 2011;94(6):1584–91.
4. Nurk E, Refsum H, Bjelland I, Drevon CA, Tell GS, Ueland PM, Vollset SE, Engedal K, Nygaard HA, Smith DA. Plasma free choline, betaine and cognitive performance: the Hordaland Health Study. Br J Nutr 2013;109(3):511–9.
5. Michel V, Yuan Z, Ramsubir S, Bakovic M. Choline transport for phospholipid synthesis. Exp Biol Med 2006;231:490–504.
6. Gareri P, Castagna A, Cotroneo AM, Putignano S, De Sarro G, Bruni AC. The role of citicoline in cognitive impairment: pharmacological characteristics, possible advantages, and doubts for an old drug with new perspectives. Clin Interv Aging 2015;10:1421–29.
7. Fioravanti M, Yanagi M. Cytidinediphosphocholine (CDP choline) for cognitive and behavioural disturbances associated with chronic cerebral disorders in the elderly. Cochrane Database Syst Rev 2005, 18;(2):CD000269, Available from: https://pubmed.ncbi.nlm.nih.gov/15846601/.
8. Eri Nakazaki, Eunice Mah, Kristen Sanoshy, Danielle Citrolo, Fumiko Watanabe. Citicoline and Memory Function in Healthy Older Adults: A Randomized, Double-Blind, Placebo-Controlled Clinical Trial. The Journal of Nutrition. 2021;151:2153–2160.
9. Owen AM. The functional organization of working memory processes within human lateral frontal cortex: the contribution of functional neuroimaging. Eur J Neurosci 1997;9(7):1329–39.
10. https://www.cambridgebrainsciences.com/science/tasks
11. Spiers PA, Myers D, Hochanadel GS, Lieberman HR, Wurtman RJ. Citicoline improves verbal memory in aging. Arch Neurol 1996;53(5):441–8.
12. Alvarez XA, Laredo M, Corzo D, Fernández-Novoa L, Mouzo R, Perea JE, Daniele D, Cacabelos R. Citicoline improves memory performance in elderly subjects. Methods Find Exp Clin Pharmacol 1997;19(3):201–10.
13. Tulving E. Episodic memory: from mind to brain. Annu Rev Psychol 2002;53:1–25.
14. Nyberg L. Functional brain imaging of episodic memory decline in ageing. J Intern Med 2017;281(1):65–74.
15. Silveri MM, Dikan J, Ross AJ, Jensen JE, Kamiya T, Kawada Y, Renshaw PF, Yurgelun-Todd DA. Citicoline enhances frontal lobe bioenergetics as measured by phosphorus magnetic resonance spectroscopy. NMR Biomed 2008;21:1066–75.
16. Grieve SM, Williams LM, Paul RH, Clark CR, Gordon E. Cognitive aging, executive function, and fractional anisotropy: a diffusion tensor MR imaging study. AJNR Am J Neuroradiol 2007;28: 226–35.
17. Hazlett EA, Buchsbaum MS, Mohs RC, Spiegel-Cohen J, Wei TC, Azueta R, Haznedar MM, Singer MB, Shihabuddin L, Luu-Hsia C, et al. Age-related shift in brain region activity during successful memory performance. Neurobiol Aging 1998;19:437–45
18. McGlade E, Agoston AM, DiMuzio J, Kizaki M, Nakazaki E, Kamiya T, Yurgelun-Todd D. The effect of citicoline supplementation on motor speed and attention in adolescent males. J Atten Disord 2019;23(2):121–34.
19. Babb SM, Wald LL, Cohen BM, Villafuerte RA, Gruber SA, YurgelunTodd DA, Renshaw PF. Chronic citicoline increases phosphodiesters in the brains of healthy older subjects: an in vivo phosphorus magnetic resonance spectroscopy study. Psychopharmacology (Berl) 2002;161:248–54.
20. Zamroziewicz MK, Zwilling CE, Barbey AK. Inferior prefrontal cortex mediates the relationship between phosphatidylcholine and executive functions in healthy, older adults. Front Aging Neurosci 2016;8: 226.
Дана інформація є узагальненою та не може використовуватись для лікування.
11COG-21-08-2023-Rx2-9.4
Коментарі (0)