Змінити пароль!
Скинути пароль!


У дослідженні застосування селаделпара були отримані перспективні результати щодо лікування первинного біліарного холангіту, раніше відомого як первинний біліарний цироз печінки.
Дані нового клінічного дослідження, в якому взяли участь пацієнти з первинним біліарним холангітом, свідчать про більш виражену біохімічну відповідь та нормалізацію активності лужної фосфатази при застосуванні селаделпара порівняно з плацебо. Крім того, при застосуванні селаделпара (агоніста дельта-рецепторів, що активуються пероксисомними проліфераторами (PPARδ)) було відмічено зниження інтенсивності свербежу середньотяжкого ступеня.
Загалом 193 пацієнти (з незадовільною відповіддю на застосування урсодіолу або розвитком побічних ефектів на застосування цього препарату в анамнезі) були рандомізовані (у співвідношенні 2 : 1) у групу лікування селаделпаром у дозі 10 мг внутрішньо щодня або у групу плацебо.
Основною кінцевою точкою дослідження було досягнення біохімічної відповіді через рік після початку лікування. Додатковими кінцевими точками були нормалізація активності лужної фосфатази (ЛФ) через один рік після початку лікування та оцінка відмінностей за показником інтенсивності свербежу через 6 місяців після початку лікування.
Із загальної кількості пацієнтів 93,8% отримували урсодіол як стандартну фонову терапію. Досягнення біохімічної відповіді у групі застосування селаделпара було відзначено у більшої кількості пацієнтів у порівнянні з групою плацебо. Крім того, у групі застосування селаделпара частіше спостерігалася нормалізація активності ЛФ (p < 0,001; див. таблицю 1).
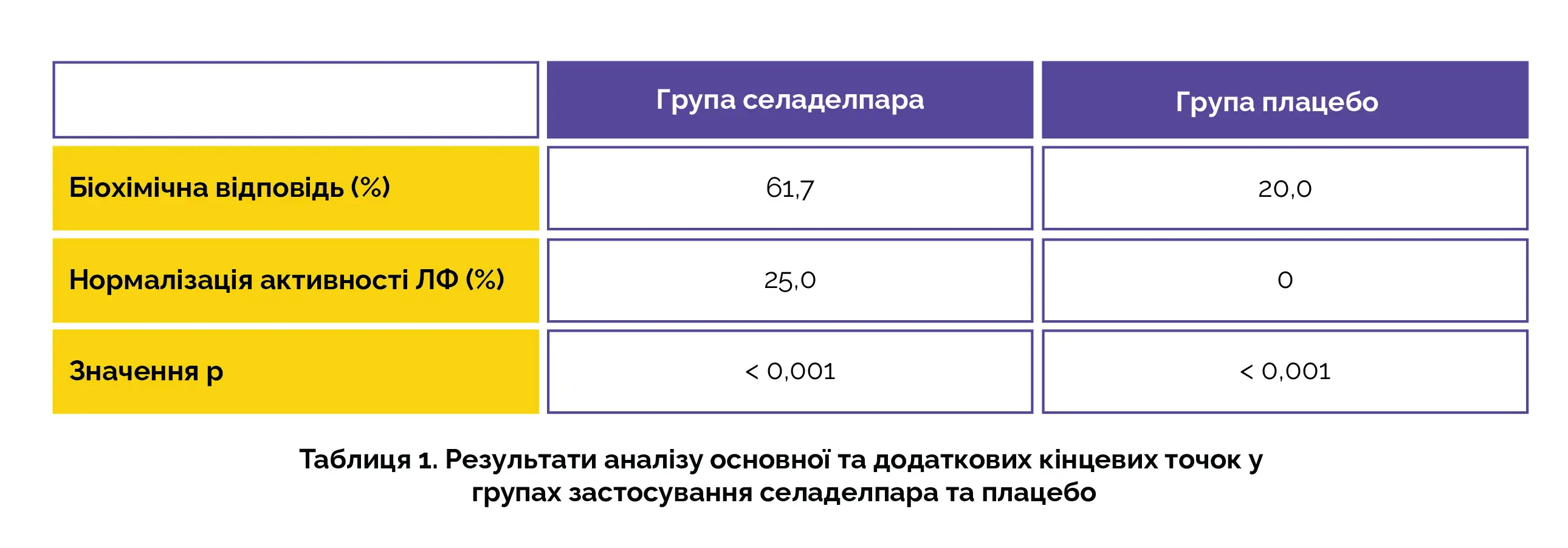
Крім цього, при застосуванні селаделпара більш вираженим було зниження інтенсивності свербежу порівняно з групою плацебо. Розвиток небажаних явищ було зареєстровано у 86,7 % та 84,6 % пацієнтів у групі застосування селаделпару та плацебо, а серйозних небажаних явищ – у 7 % та 6,2 % пацієнтів відповідно.
The New England Journal of Medicine
A Phase 3 Trial of Seladelpar in Primary Biliary Cholangitis
Gideon M Hirschfield і співавт.
Коментарі (0)