Змінити пароль!
Скинути пароль!


Близько 40% світового населення страждають на алергічний риніт. Характерними проявами алергічного риніту є такі рецидивні симптоми, як закладеність носа, ринорея, свербіж у носі та чхання.
Застосування сублінгвальної імунотерапії алергенами кліщів домашнього пилу у формі таблеток для симптоматичного лікування алергічного риніту є безпечним та ефективним та дозволяє підвищити якість життя пацієнтів.
Близько 40% світового населення страждають на алергічний риніт. Характерними проявами алергічного риніту є такі рецидивні симптоми, як закладеність носа, ринорея, свербіж у носі та чхання. Це захворювання також має великий вплив з економічної точки зору, включаючи прямі та опосередковані витрати на лікування, втрату продуктивності праці та погіршення якості життя. До стандартних методів контролю алергічного риніту відносяться лікарська терапія та уникнення впливу алергенів. Перспективним варіантом лікування у осіб з рефрактерністю до лікарської терапії було визнано алерген-специфічну імунотерапію (АСІТ).
АСІТ дозволяє модулювати імунну відповідь і в даний час вважається єдиним варіантом лікування з можливістю модифікації захворювання у довгостроковій перспективі. Стандартні методи проведення АСІТ включають сублінгвальну (СЛІТ) та підшкірну (ПШІТ) алергенспецифічну імунотерапію. Ефективність обох методів була підтверджена результатами численних мета-аналізів та рандомізованих контрольованих досліджень (РКД). Метод СЛІТ набув своєї популярності завдяки простоті застосування та високому рівню безпеки. СЛІТ проводять із застосуванням препаратів у формі таблеток або крапель. Все частіше перевагу віддають лікарським формам у вигляді таблеток, а не крапель, оскільки дана форма проста у застосуванні, забезпечує більш надійне дозування алергену, а її клінічна ефективність підтверджена науковими даними.
Два основні види кліщів домашнього пилу (далі - КДП, найпоширеніший алерген у всьому світі) - Dermatophagoides farinae і Dermatophagoides pteronyssinus. Роль алергенів КДП у розвитку алергічного риніту та бронхіальної астми добре вивчена. Результати різних мета-аналізів даних подвійних сліпих плацебо-контрольованих досліджень застосування СЛІТ та ПШІТ у дітей та дорослих з алергічною бронхіальною астмою та алергічним ринітом вказують на ефективність АСІТ з КДП у осіб із захворюваннями дихальної системи алергічної етіології. Встановлено, що застосування АСІТ з КДП є ефективним та супроводжується підвищенням якості життя, зменшенням обсягу застосування резервних препаратів та зниженням виразності симптомів захворювання.
Однак, кінцеві точки, лікарські форми для проведення АСІТ, демографічні характеристики досліджуваних популяцій та дизайн клінічних досліджень характеризуються високим ступенем неоднорідності. Результати непрямого порівняння ПШІТ з КДП та СЛІТ із КДП у рамках мережевого мета-аналізу вказують, що перший варіант терапії перевершує СЛІТ, забезпечуючи більш ефективне зниження виразності симптомів алергічного риніту. Однак, на відміну від застосування СЛІТ у таблетках, яке вивчали у великих подвійних сліпих плацебо-контрольованих дослідженнях з якісним дизайном, кількість учасників у РКД з оцінки застосування ПШІТ та СЛІТ у краплях була дуже низькою. Дослідження ПШІТ та СЛІТ у формі крапель також відрізнялися високою неоднорідністю щодо застосовуваних препаратів алергенів, їх дозувань та кінцевих точок.
Згідно з нещодавно випущеними рекомендаціями Європейської академії алергології та клінічної імунології (EAACI) як основну кінцеву точку в дослідженнях АСІТ слід використовувати показники уніфікованої шкали оцінки назальних симптомів риніту з урахуванням потреб у лікарських препаратах (CSMS). У деяких регіонах світу до застосування були схвалені лише два препарати для СЛІТ з КДП у формі таблеток зі стандартизацією із застосуванням індексу реактивності (ІР) та таблеток стандартної якості (SQ-HDM).
ОБГРУНТУВАННЯ ДОСЛІДЖЕННЯ
Мета-аналізи даних про ефективність застосування СЛІТ у формі таблеток у пацієнтів з алергічним ринітом, викликаним алергенами КДП, з використанням оцінки за шкалою CSMS як основної кінцевої точки, раніше не проводилися. У зв'язку з цим було проведено даний систематичний огляд та мета-аналіз.
МЕТА
Мета дослідження полягала в оцінці ефективності застосування СЛІТ у формі таблеток з урахуванням таких показників, як оцінка виразності кон'юнктивіту, симптомів риніту, обсягу застосування лікарських препаратів, безпеки та якості життя у пацієнтів з алергічним ринітом, викликаним алергенами КДП.
Пошук літератури
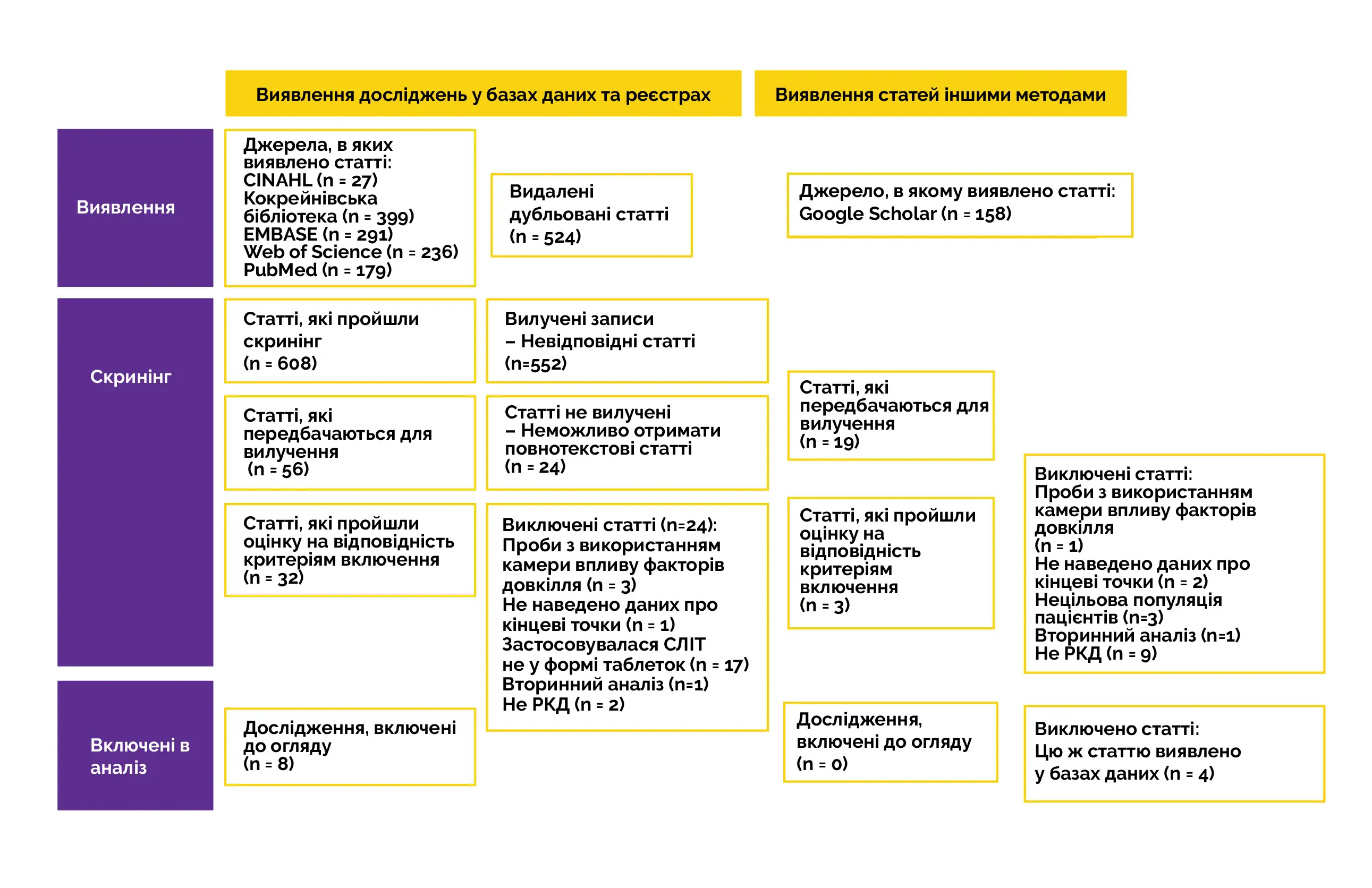
Пошук відповідної літератури проводили у п'яти електронних базах даних, включаючи CINAHL, Кокрейнівський центральний реєстр контрольованих досліджень, Web of Sciences, EMBASE та PubMed. Для виявлення відповідної літератури застосовували підхід із структурованим пошуком. При пошуку в кожній базі даних використовували специфічну затверджену термінологію, наприклад, Медичні предметні рубрики (MeSH) при пошуку в базі даних PubMed. Виявлення літератури, що не індексована в медичних базах даних, виконували за допомогою розширеного пошуку в системі Google Scholar, що дозволяє отримати додаткові роботи, правами на які володіють комерційні видавництва, а також неопубліковані роботи. З іншого боку, для виявлення інших відповідних робіт проводили аналіз списку літератури кожної публікації.
Критерії включення
В аналіз включали РКД з будь-яким розміром вибірки за умови їх відповідності наступним критеріям:
Критерії виключення
Дослідження виключали з аналізу за їх відповідності наступним критеріям:
Відбір досліджень та вилучення даних
Заголовки та анотації всіх виявлених робіт, відповідних критеріям включення, було розглянуто двома авторами. При виключенні дослідження з аналізу проводили зіставлення та обговорення причин такого виключення. Будь-які розбіжності вирішувалися у рамках зустрічі з третім автором. Два автори незалежно один від одного вилучали з публікацій такі дані: основні результати, кінцеві точки, розмір вибірки, особливості втручання та контролю, характеристики пацієнтів, критерії включення та виключення, дизайн дослідження, країна, рік публікації та авторство.
Вилучені дані перевіряли ще раз, і за наявності будь-яких розбіжностей проводили узгодження з третім автором. За відсутності необхідних даних у достатньому обсязі відповідним дослідникам надсилали листи електронною поштою. Якщо протягом двох тижнів відповіді не надходило, дані реєстрували як відсутні або відновлювали. Точне середнє значення зі стандартним відхиленням (СВ) розраховували за даними повної вибірки для аналізу (FAS), при цьому для вивчення безперервних змінних (наприклад, оцінки за шкалою CSMS і оцінки за шкалою виразності симптомів риніту (RSS)) вилучали дані про кількість учасників.
З публікацій, в яких були представлені лише середні значення та СВ, дані вилучали за допомогою інструменту Digitizelt. Для визначення середніх значень та СВ для публікацій, в яких були представлені значення медіани та міжквартильний розмах, використовували методику Wan та співавт. Відповідно до рекомендацій, викладених у Кокрейнівському посібнику з систематичних оглядів, якщо СВ для значень не було наведено, робили його підстановку з використанням 95 % різниці значень між групами плацебо та СЛІТ з КДП. Для аналізу бінарних змінних, таких як показники безпеки та загальна оцінка, вилучали дані про кількість пацієнтів, які повідомили про зниження виразності симптомів та значне поліпшення самопочуття після завершення терапії. Для вивчення безпеки вилучали дані про кількість учасників, у яких спостерігався розвиток небажаних явищ, пов'язаних з лікуванням, у кожній групі дослідження.
Дані та статистичний аналіз
Для всіх статистичних аналізів використовували пакет спеціалізованих програм Stata версії 17. Статистичну значущість визначали при досягненні двостороннього значення р менше 0,05. В рамках мета-аналізу для визначення середніх значень та 95% довірчих інтервалів (ДІ) за об'єднаними даними використовували модель з випадковими ефектами Дерсіміана та Лерда. Для об'єднання даних за безперервними змінними, такими як оцінка за шкалою CSMS, які являють собою безперервні дані з різними шкалами вимірювання, використовували стандартизовану різницю середніх (СРС).
Для встановлення ефектів лікування щодо СРС використовували визначення ефектів лікування Коена для значних інтерпретацій; при сукупній різниці, що дорівнює 0,2, 0,5 і 0,8, ефект лікування вважали невеликим, середнім або виразним відповідно. Для узагальнення даних за такими бінарними кінцевими точками, як прийнятність лікування та показники безпеки, використовували значення відносного ризику (ВР) та 95% ДІ за об'єднаними даними. Для визначення неоднорідності даних використовували коефіцієнт I2, діапазон значень якого починається з 0% і закінчується 100%, причому більш високі значення вказують на більш високий рівень варіабельності показників досліджень. Значення коефіцієнта I2, рівні 75%, 50% і 25%, вказують на високу, середню та низьку неоднорідність даних відповідно.
Крім того, був виконаний аналіз у підгрупах учасників, які отримували препарати для СЛІТ з КДП у дозах 500 ІР/мл, 300 ІР/мл, 12 SQ-HDM або в еквівалентній дозі (20 000 японських алергенних одиниць (ЯАЕ)) або 6 SQ-HDM або в еквівалентній дозі (10 000 ЯАЕ) у формі сублінгвальних таблеток. Цих пацієнтів розділили на чотири групи з урахуванням віку (діти віком 5–11 років та учасники ≥12 років) та дози препарату. Усі результати мета-аналізу були представлені у вигляді форест-діаграм. Для виключення систематичної помилки, пов'язаної з переважною публікацією позитивних результатів досліджень, були побудовані лійкоподібні графіки.
Оцінка ризику систематичних помилок та оцінка якості
Оцінку методологічної якості включених у аналіз досліджень виконували два автори незалежно друг від друга, причому у разі розбіжностей задля досягнення консенсусу проводили обговорення з третім автором. Для визначення якості кожного дослідження використовували алгоритм оцінки наявності систематичних помилок (RoB2) Кокрейнівської групи з вивчення якості РКД.
Оцінку методологічної якості виконували за п'ятьма доменами:
1) систематичні помилки, пов'язані з процедурою рандомізації;
2) систематичні помилки, пов'язані з відхиленням від встановленого режиму лікування;
3) систематичні помилки, пов'язані з відсутністю даних про кінцеві точки;
4) систематичні помилки внаслідок неправильної оцінки кінцевих точок;
5) систематичні помилки, пов'язані з вибірковою публікацією результатів.
В рамках аналізу з використанням алгоритму RoB2 кожному дослідженню надавали відповідну оцінку.
Кінцеві точки дослідження
Показники
Характеристики досліджень та учасників:
Якість досліджень
Щодо якості, ризик виникнення систематичних помилок у 7 досліджень був визнаний низьким.
Сумніви виникли лише щодо одного дослідження, оскільки були відсутні дані про кінцеві точки.
Вплив втручання на кінцеві точки
У цей систематичний огляд даних про застосування СЛІТ з КДП у формі таблеток були включені 8 плацебо-контрольованих подвійних сліпих РКД з достатнім обсягом інформації. СЛІТ із КДП у формі таблеток отримав 3601 учасник, а плацебо – 2783 учасника. У дітей, підлітків та дорослих, які отримували СЛІТ з КДП у формі таблеток, було відзначено статистично значуще зниження виразності клінічних симптомів риніту та обсягу застосування лікарських препаратів, що вимірювали за допомогою оцінки RMS та оцінок за шкалою CSMS та за шкалою RSS. Крім того, цей варіант лікування був безпечним і забезпечував зниження симптомів кон'юнктивіту та підвищення якості життя. Даний мета-аналіз являє собою перший мета-аналіз, присвячений вивченню оцінки за шкалою CSMS як основної кінцевої точки відповідно до рекомендацій EAACI.
При оцінці об'єднаних даних за основною кінцевою точкою при застосуванні СЛІТ з КДП у формі таблеток СРС склала -0,28 (95% ДІ: від -0,33 до -0,23). На тлі СЛІТ з КДП у формі таблеток зі стандартизацією із застосуванням ІР та таблеток стандартної якості SQ-HDM спостерігалася стабільна ефективність терапії при застосуванні відповідних препаратів у різних дозах (6 SQ-HDM, 12 SQ-HDM, 300 ІР/мл та 500 ІР/ мл), при цьому різниці між результатами досліджень були мінімальними. При проведенні аналізу у підгрупах щодо клінічної відповіді на лікування, яку вимірювали за допомогою оцінки за шкалами RSS та CSMS, відмінностей у групах дослідження виявлено не було. Згідно з визначенням Всесвітньої алергологічної організації (ВАО), мінімальний статистично значущий вплив АСІТ – різниця за показником клінічного покращення понад 20 % порівняно з плацебо. У зв'язку з відсутністю даних визначити сукупну різницю за показником клінічного поліпшення неможливо.
У РКД з трьома групами, у яких брали участь 992 дорослих пацієнтів з алергічним ринітом, які отримували досліджуваний препарат у формі таблеток у дозі 6 SQ-HDM або 12 SQ-HDM або плацебо, результати були більш багатообіцяючими при застосуванні препаратів у формі таблеток у дозі 12-HDM (відносна різниця оцінок TCRS в порівнянні з плацебо 22% проти 18% при дозі 6 SQ-HDM). Цей висновок залишився без змін навіть з огляду на те, що клінічно значуще покращення порівняно з плацебо спостерігалося при застосуванні препаратів для СЛІТ з КДП у різних дозах. При застосуванні препарату для СЛІТ з КДП у дозі 12 SQ-HDM було виявлено зниження значень по всіх додаткових кінцевих точках, включаючи оцінку за шкалою RSS, оцінку RMS та комбіновану оцінку виразності ринокон'юнктивіту, а також покращення якості життя.
Очевидно, це і спричинило надання дозволу на застосування препарату для СЛІТ з КДП у формі таблеток у дозі 12 SQ-HDM для лікування дорослих та підлітків з алергічним ринітом. У двох дослідженнях брали участь діти віком до 12 років (повна популяція дітей включала пацієнтів віком від 5 до 18 років). Результати цих РКД свідчили про хорошу переносимість та ефективність застосування препаратів для СЛІТ з КДП у формі таблеток у дозі 6 SQ-HDM та 300 ІР/мл у дітей молодшого віку. У порівнянні з підлітками та дорослими, дітям, мабуть, потрібна нижча ефективна доза препаратів для СЛІТ з КДП. У всіх включених до аналізу дослідженнях зниження оцінки RMS на фоні застосування СЛІТ з КДП було менш виразним, ніж оцінки за шкалою RSS. Це може вказувати на те, що поліпшення клінічного стану не завжди достатньо корелює із застосуванням знеболювальних препаратів за потребою.
Використання лише оцінок, пов'язаних із впливом препарату, для визначення клінічної ефективності АСІТ може призвести до переоцінки справжнього впливу цієї терапії на результати. У Керівництві Європейського агентства з лікарських засобів (EMA) 2008 року зазначено, що оцінка АСІТ у рамках досліджень ІІІ фази має проводитися в умовах впливу природних факторів (тобто в умовах проб у реальних умовах). Камеру для впливу алергену можна використовувати тільки при проведенні досліджень І та ІІ фази або для підтвердження результатів досліджень ІІІ фази в умовах реальних клінічної практики. Тому дослідження, в яких для оцінки основної кінцевої точки проводили провокаційні проби з алергеном, наприклад з використанням спеціальних камер для впливу алергену, виключали з аналізу.
Вивчення впливу СЛІТ із КДП у формі таблеток на симптоми з боку очей з використанням оцінки TCCS було виконано лише у трьох дослідженнях. Результати цього мета-аналізу підтвердили висновок раніше проведеного систематичного огляду про те, що при застосуванні СЛІТ у осіб з алергічним ринокон'юнктивітом може спостерігатися зниження як загальної, так і окремих оцінок симптомів з боку очей. Загальна оцінка поліпшення стану пацієнтами в рамках вивчення ефективності втручання була статистично значуще вищою за активного лікування порівняно з плацебо (ВР: 1,21 (95 % ДІ: 1,14–1,29)). Порівняно з плацебо, у групі активного лікування також спостерігалося зниження оцінки за опитувальником RQLQ (СРС: −0,23 (95 % ДІ: від −0,29 до −0,16)), що свідчить про підвищення якості життя. Ефективність застосування СЛІТ з КДП у формі таблеток також була підтверджена результатами оцінки всіх об'єднаних даних з помірною та низькою неоднорідністю.
На відміну від ПШІТ, дані моніторингу безпеки застосування СЛІТ у формі таблеток протягом тривалого періоду відсутні. Однак наявні дані вказують, що застосування СЛІТ може бути безпечнішим, ніж застосування ПШІТ. Незважаючи на те, що при застосуванні СЛІТ спостерігалися деякі місцеві небажані явища, розвиток серйозних системних побічних ефектів відбувається нечасто. У клінічних дослідженнях застосування СЛІТ у формі таблеток у США настання смертельних випадків зареєстровано не було. Адреналін вводили лише 35 учасникам (0,2 % від 8152 випадків розвитку небажаних явищ, пов'язаних із застосуванням СЛІТ). У жодному випадку небажане явище не було високого рівня ризику чи загрозливим життя. Відповідно до результатів цього систематичного огляду частота розвитку небажаних явищ, пов'язаних із застосуванням досліджуваного препарату, у групі лікування була набагато вищою, ніж у групі плацебо (65,1 % порівняно з 22,7 %). Частота розвитку небажаних явищ тяжкого ступеня становила 0,3%.
У ході проведення досліджень адреналін вводили 8 учасникам із групи лікування (0,20 %); це свідчить про порівнянну частоту його застосування проти групи плацебо (7 учасників; 0,24 %). Незважаючи на те, що системні реакції на застосування СЛІТ виникають рідко, причиною припинення лікування часто є неприємні місцеві побічні ефекти. Згідно з результатами цього мета-аналізу, у пацієнтів, які отримують СЛІТ з КДП у формі таблеток, ймовірність припинення лікування через розвиток НЯ, пов'язаних із застосуванням препарату, статистично значуще вище (ВР: 2,09; 95 % ДІ: 1,27–3,44 ).
Тривалість клінічних досліджень СЛІТ з КДП у формі таблеток становила лише один рік, незважаючи на те, що згідно з поточними стандартами застосування СЛІТ рекомендується продовжувати протягом не менше трьох років. Стійке зниження виразності симптомів протягом другого року було встановлено у подвійному сліпому РКД тривалістю 2 роки із застосуванням СЛІТ з КДП у формі таблеток протягом 1-го року та спостереженням протягом 2-го року на тлі відсутності лікування. У зв'язку з цим може виникнути питання про те, чи дійсно лікування має тривати протягом трьох років.
У подвійному сліпому великому плацебо-контрольованому дослідженні з якісним дизайном дітей з алергічним ринітом лікували із застосуванням таблеток для СЛІТ із пилковими алергенами трав протягом трьох років. У дітей, які отримували лікування, через 2 роки після припинення СЛІТ було виявлено стійке зниження симптомів алергічного риніту, статистично значуще зниження симптомів бронхіальної астми та обсягу застосування лікарських препаратів. Залишається незрозумілим, чи дозволяє СЛІТ у формі таблеток з іншими алергенами забезпечити такий же тривалий ефект лікування та модифікацію перебігу захворювання. Для вивчення ефективності застосування СЛІТ з КДП у формі таблеток та її контролю необхідно провести більш тривалі РКД.
Підсумовуючи, відзначимо, що результати цього систематичного огляду та мета-аналізу вказують на ефективність застосування СЛІТ з КДП у формі таблеток щодо полегшення симптомів алергічного риніту та мінімізації обсягу застосування лікарських препаратів. Це лікування також забезпечувало зниження виразності симптомів кон'юнктивіту та підвищення якості життя. При цьому його ефективність була встановлена у пацієнтів з алергічним ринітом віком від 5 років. Незважаючи на те, що розвиток небажаних явищ, пов'язаних з лікуванням, відбувається часто, більшість з них є тимчасовими і мають легкий ступінь тяжкості.
У разі розвитку серйозних небажаних явищ адреналін застосовували нечасто. Незважаючи на те, що СЛІТ з КДП у формі таблеток вважається безпечним та ефективним варіантом лікування, її застосування в реальній клінічній практиці в деяких країнах досі дуже обмежене. Серйозними перешкодами є тривалість лікування, відсутність доступу до препаратів, їхня висока вартість, недостатня обізнаність пацієнтів та відсутність досвіду проведення СЛІТ у лікарів-практиків.
У осіб з алергічним ринітом застосування СЛІТ з КДП у формі таблеток є безпечним і забезпечує ефективне полегшення симптомів риніту, кон'юнктивіту та обсягу застосування лікарських препаратів. Крім того, це лікування дозволяє підвищити якість життя пацієнтів.
World Allergy Organization Journal
Efficacy and safety of house dust mite sublingual immunotherapy tablets in allergic rhinitis: A systematic review and meta-analysis
Prapasri Kulalert і співавт.
Коментарі (0)