Змінити пароль!
Скинути пароль!


Було проведено багатогрупове рандомізоване подвійне сліпе плацебо-контрольоване дослідження IIIb фази для оцінки ефективності та безпеки застосування ептинезумабу, моноклонального антитіла, для профілактики мігрені у пацієнтів із цим захворюванням, у яких 2-4 попередні спроби профілактичного лікування були неуспішними.
У пацієнтів з мігренню, у яких 2-4 попередні спроби профілактичного лікування були неуспішними, застосування ептинезумабу безпечне, добре переноситься та забезпечує виразний профілактичний ефект щодо мігрені порівняно з плацебо.
Було проведено багатогрупове рандомізоване подвійне сліпе плацебо-контрольоване дослідження IIIb фази для оцінки ефективності та безпеки застосування ептинезумабу, моноклонального антитіла, для профілактики мігрені у пацієнтів із цим захворюванням, у яких 2-4 попередні спроби профілактичного лікування були неуспішними.
Дослідження DELIVER складалося з 24-тижневого плацебо-контрольованого подвійного сліпого періоду та 48-тижневого додаткового періоду з приховуванням даних про призначену дозу. До дослідження включали дорослих пацієнтів з епізодичною або хронічною мігренню, у яких кількість днів з нападом мігрені на місяць становила не менше чотирьох і протягом попередніх 10 років 2-4 спроби профілактичного лікування завершилися невдачею.
Рандомізацію пройшов загалом 891 пацієнт, який отримав як мінімум одну дозу досліджуваного препарату. Популяція для оцінки безпеки ептинезумаба в дозі 100 мг становила 34 % (n = 299), ептинезумаба 300 мг - 33 % (n = 294), група плацебо - 33 % (n = 298). Рандомізацію проводили з використанням централізованої системи зі стратифікацією по країнах та початковій кількості днів із нападом мігрені на місяць.
Основною кінцевою точкою оцінки ефективності за даними повної вибірки для аналізу була зміна кількості днів з нападом мігрені на місяць відносно вихідного рівня з 1-го по 12-й тиждень дослідження. Весь персонал дослідження та всі його учасники не мали доступу до даних про призначене лікування.
Плацебо-контрольований період дослідження повністю пройшли 865 пацієнтів. У таблиці 1 наведено дані про зміну кількості днів з нападом мігрені на місяць відносно вихідного рівня з 1-го по 12-й тиждень та про частоту розвитку побічних ефектів при застосуванні ептинезумабу у дозі 100 мг, ептинезумабу у дозі 300 мг та плацебо.
Найбільш частим небажаним явищем, що виникло під час лікування, був COVID-19. Важкі небажані явища розвивалися нечасто і включали анафілактичну реакцію (ептинезумаб 300 мг, n = 2) і COVID-19 (ептинезумаб 100 мг, n = 1 і ептинезумаб 300 мг, n = 1).
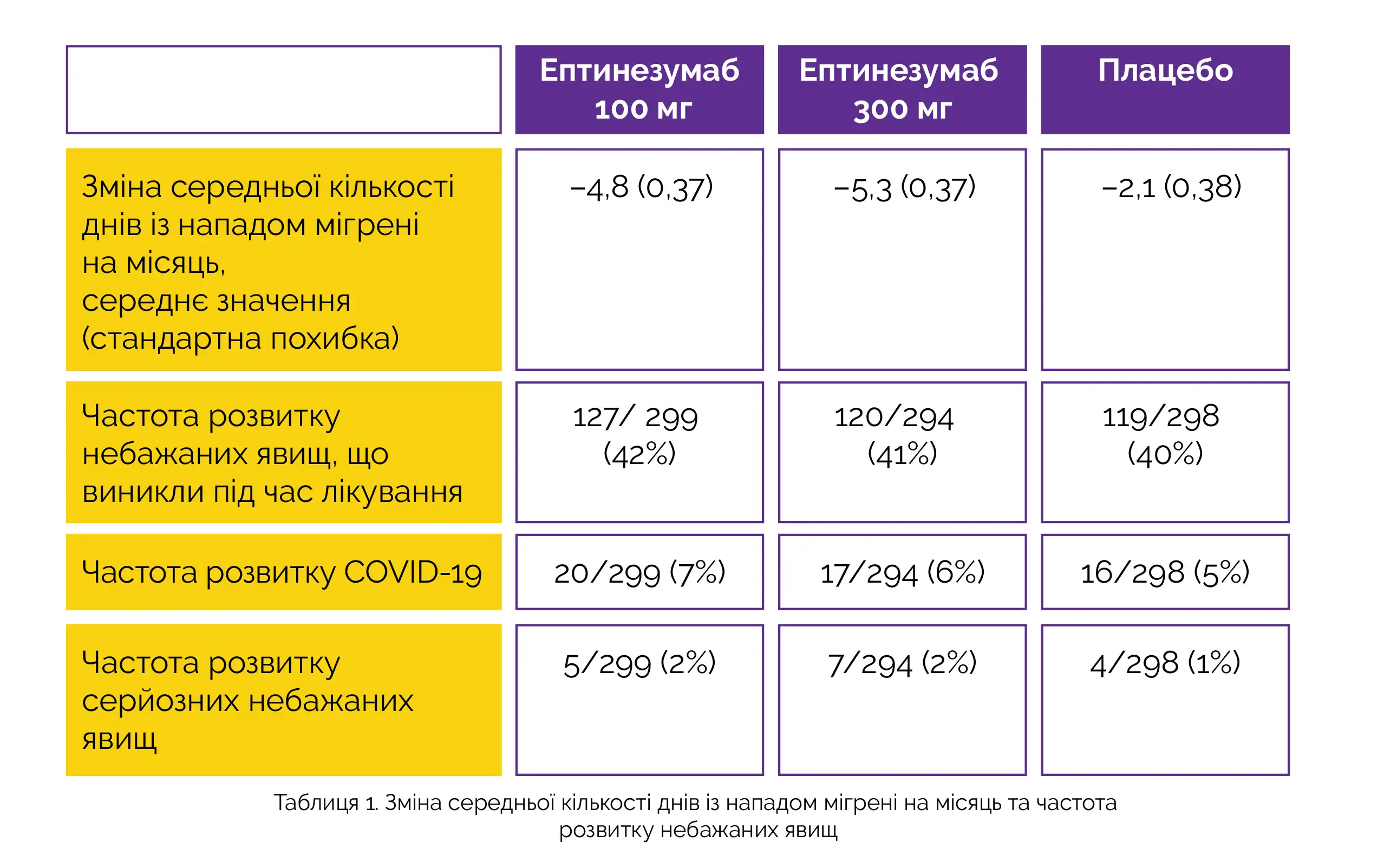
При застосуванні ептинезумабу в дозі 100 мг і 300 мг зміна середньої кількості днів з нападами мігрені на місяць відносно вихідного рівня статистично значуще відрізнялася від такої в групі плацебо.
Застосування ептинезумабу – ефективний варіант лікування у пацієнтів з мігренню, що характеризується сприятливим профілем безпеки та переносимості.
Lancet Neurology
Safety and efficacy of Eptinezumab for migraine prevention in patients with two-to-four previous preventive treatment failures (DELIVER): a multi-arm, randomised, double-blind, placebo-controlled, phase 3b trial
Prof Messoud Ashina і співавт.
Коментарі (0)