Змінити пароль!
Скинути пароль!


Метою проведеного проспективного багатоцентрового рандомізованого контрольованого дослідження було визначення ефективності та безпеки переходу з ентекавіру на тенофовіру алафенаміду фумарат.
У пацієнтів з хронічним вірусним гепатитом В ефект переходу з ентекавіру на тенофовіру алафенаміду фумарат на концентрацію поверхневого антигену вірусу гепатиту B у сироватці крові та функцію нирок можна порівняти з продовженням застосування ентекавіру.
Метою проведеного проспективного багатоцентрового рандомізованого контрольованого дослідження було визначення ефективності та безпеки переходу з ентекавіру на тенофовіру алафенаміду фумарат.
У дослідженні було рандомізовано 30 пацієнтів. З них 14 пацієнтів (3 жінки та 11 чоловіків; медіана віку: 60 років) пройшли оцінку у складі групи, яка продовжила отримання ентекавіру, та 16 пацієнтів (9 жінок та 7 чоловіків; медіана віку: 63 роки) — у складі групи, яку перевели на лікування тенофовіром. Пацієнти отримували ентекавір внутрішньо в дозі 0,5 мг на добу натще або тенофовіру алафенаміду фумарат внутрішньо в дозі 25 мг на добу після прийому їжі. Протягом 24 місяців пацієнти виконували візити з частотою один раз на 3 місяці, при цьому клінічну інформацію збирали на візитах через 3, 6, 9, 12, 18 та 24 місяці після включення до дослідження.
Основною кінцевою точкою в дослідженні була зміна концентрації поверхневого антигену вірусу гепатиту B (HBsAg) та нормалізація концентрації HBsAg у сироватці крові через 24 місяці, при цьому додатковими кінцевими точками були стійка нормалізація концентрації ДНК вірусу гепатиту B (ВГВ) у сироватці крові, зміна активності аланінамінотрансферази (АЛТ), зникнення HBeAg із сироватки крові, розрахункова швидкість клубочкової фільтрації (рШКФ) та концентрація неорганічного фосфору. Статистичний аналіз проводили за допомогою комп'ютерної програми JMP 14.2. Для міжгрупового порівняння частот використовували критерій хі-квадрат, а для порівняння безперервних змінних — критерій суми рангів Вілкоксона.
У всіх пацієнтів концентрація ДНК ВГВ у сироватці крові була нижчою за поріг виявлення. Через 2 роки між групами застосування ентекавіру та тенофовіру статистично значущих відмінностей (−0,20 порівняно з −0,08 log МЕ/мл) за показником середньої зміни концентрації HbsAg виявлено не було. Результати загального аналізу вказували, що тривалість попереднього прийому ентекавіру у групі зі зниженням концентрації HBsAg (до -0,1 log МЕ/мл або менше) була статистично значно меншою порівняно з групою без зниження концентрації HBsAg (49 порівняно з 92 місяцями).
У порівнянні з групою застосування ентекавіру, у пацієнтів із групи застосування тенофовіру спостерігалася тенденція до більш виразного зниження значень рШКФ (-6,15 порівняно з -2,26 мл/хв/1,73 м2). Однак статистично значущих відмінностей серед осіб з вихідними значеннями рШКФ нижче 60 (0,40 порівняно з −2,49 мл/хв/1,73 м2) не виявлено (див. малюнок 1).
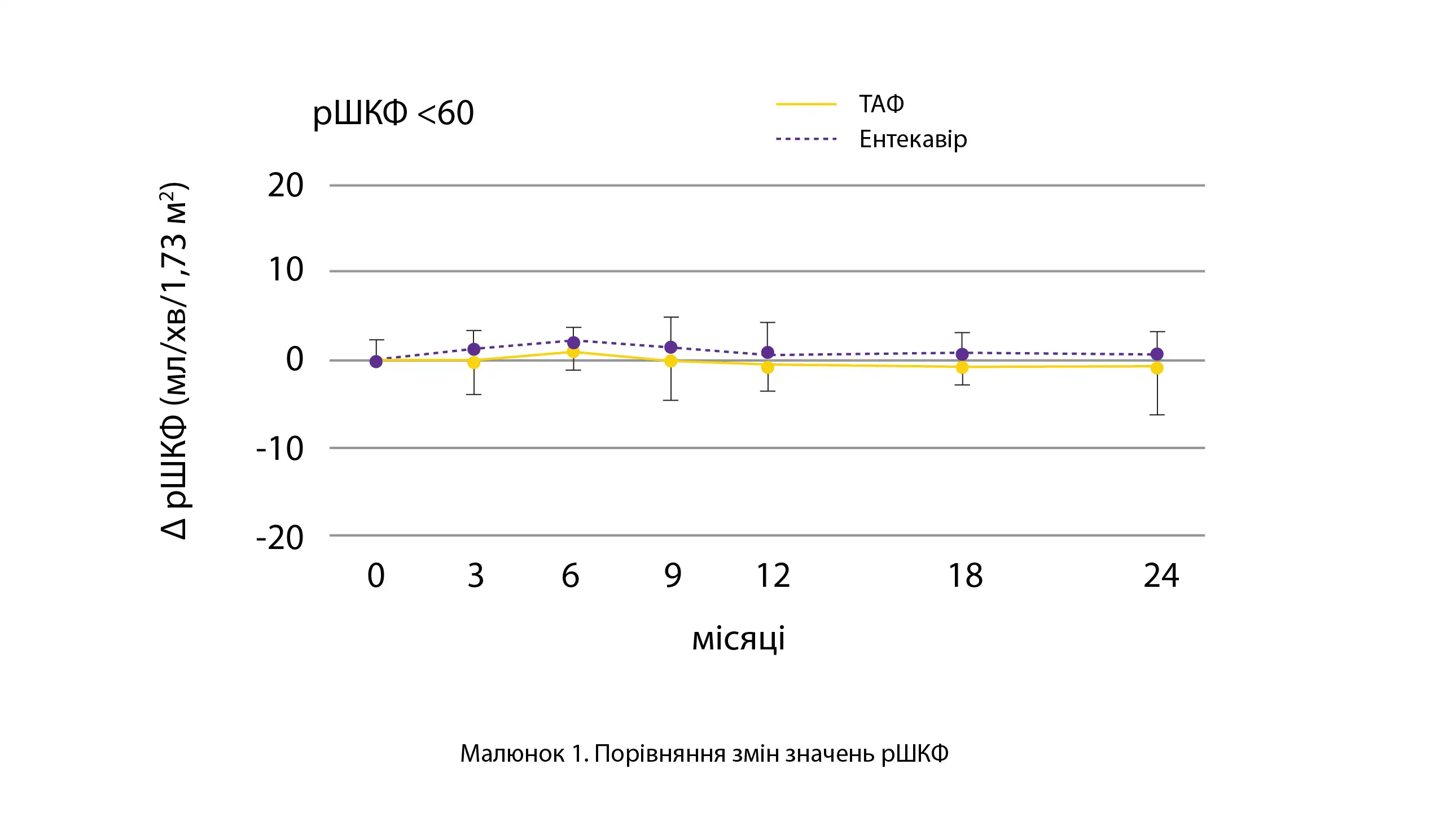
Таким чином, ефективність та безпека лікування у групах переходу на тенофовір та продовження прийому ентекавіру були порівнянними.
Medicine (Baltimore)
Switching to Tenofovir alafenamide versus continued therapy in chronic hepatitis B patients who were treated with entecavir: A prospective, multicenter, randomized controlled study
Kosuke Sato і співавт.
Коментарі (0)